TGF-βファミリーシグナル異常がもたらす疾患の解明
はじめに
私達は、なぜ様々な病気に罹患するのでしょうか?TGF-β (Transforming growth factor-β)ファミリーは、多彩な機能を持つサイトカインで、その生理作用は細胞増殖、細胞死、細胞分化、免疫調節、細胞運動等多岐に及んでいます。そのため、TGF-βファミリーシグナルに関与する分子の遺伝子異常は、様々な疾患を引き起こします。私達は、TGF-βシグナルの異常により引き起こされる疾患の分子メカニズムを解明することで、くすりの開発を通じて人間社会に少しでも貢献できるよう、日夜頑張っています。
研究室メンバー
教授 伊東 進
准教授 田所 悦
講師 中野 なおこ
研究生 1名
博士課程 1名
修士課程 1名
6年生 20名
5年生 16名
4年生 15名
大学院生募集
現在、私たちの研究室では、大学院生(博士課程、社会人博士課程、修士課程を募集しております。がんの分子生物学研究・シグナル伝達研究、特に「TGF-βシグナル伝達とがん進展」に興味がある方は、是非ともメールにてお問い合わせください。
博士課程は、TA採用により学費は実質無料となる制度があります。
社会人博士課程には、早期修了制度があります。
博士・修士課程の学費は国公立大の水準です。海外や日本国内在住の国費・私費留学生も受け入れております。私費留学生には、基準を満たせば、授業料減額のサポートもあります。
お問い合わせ先:生化学研究室 教授 伊東 進
(メールアドレス sitohアットマークac.shoyaku.ac.jp)アットマークを@に変換してください。
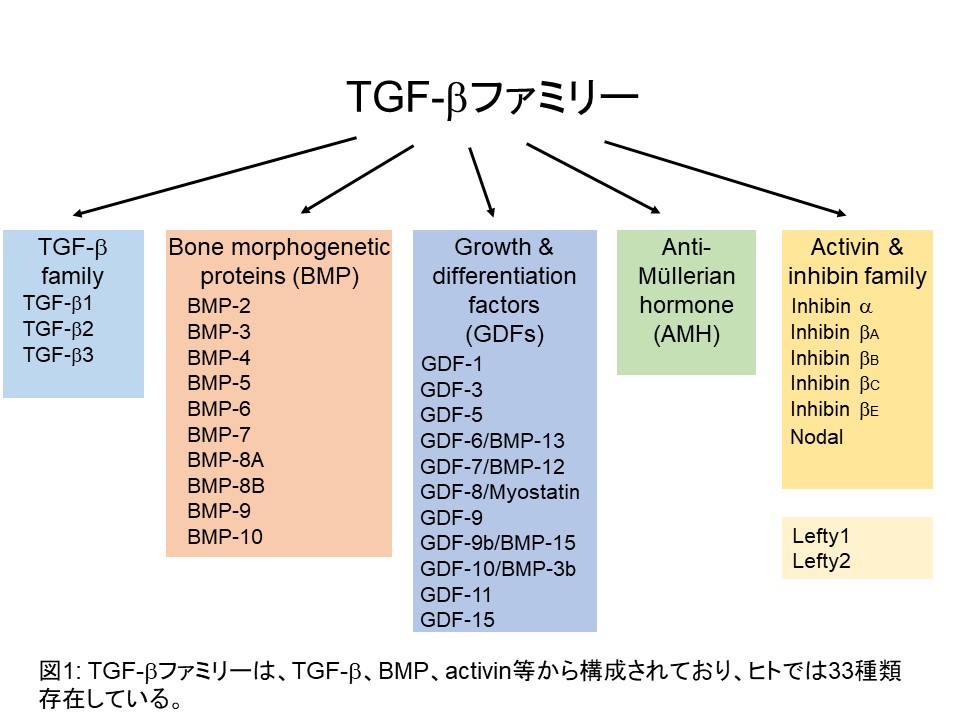
TGF-βは、アクチビンやBMPとファミリーを形成し、現在ヒトにおいて、33種類のファミリー分子から構成されています(図1)。
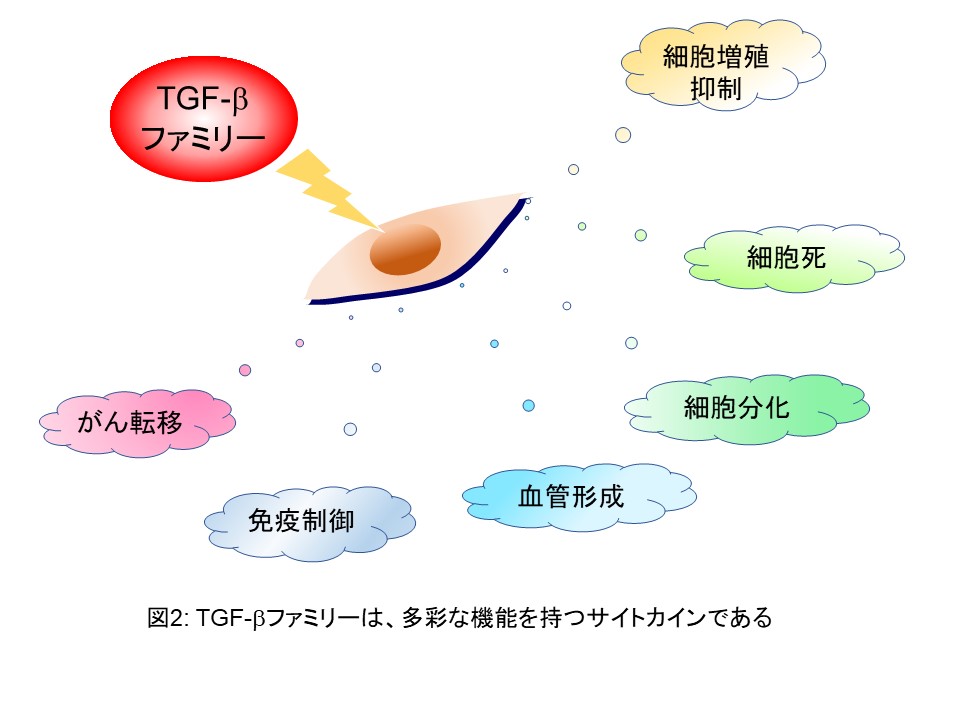
TGF-βは、多くの上皮細胞や血球系細胞の増殖を抑制する作用を有しており、TGF-βシグナルに関連するタンパク質の遺伝子変異ががん化に関与しています。細胞増殖抑制作用以外にもアポトーシス、細胞分化、免疫調節、細胞運動、血管新生等を制御しており(図2)、発生直後の胎生期より成熟個体まで様々な組織・臓器で作用をもたらす生体にとって必須のシグナル系です。
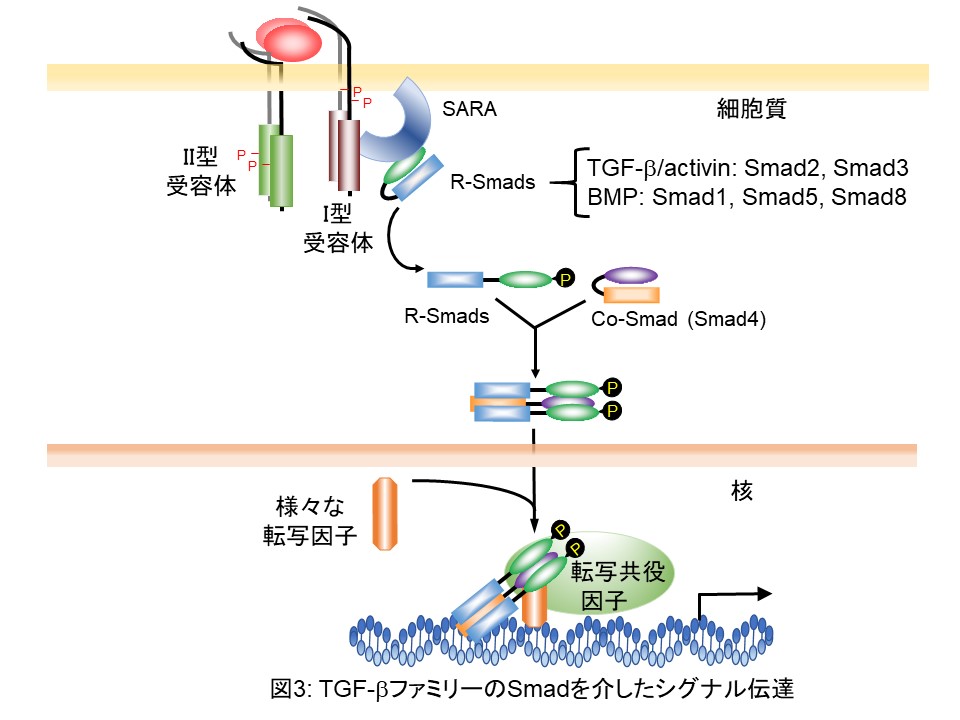
TGF-βは、細胞膜上に存在している膜貫通型受容体のTGF-β II型受容体とTGF-β I型受容体に結合します。TGF-βⅡ型並びにTGF-βⅠ型受容体は、共にその細胞内領域内にセリン・トレオニンキナーゼドメインを有しております。TGF-βがTGF-βⅡ型受容体と結合するとTGF-βⅡ型受容体セリン・トレオニンキナーゼがTGF-βⅠ型受容体の細胞膜直下に存在するセリンやトレオニンに富んだGSドメインとよばれる領域をリン酸化します。TGF-βⅠ型受容体がリン酸化されると、今まで不活性化状態で存在していたTGF-βⅠ型受容体セリン・トレオニンキナーゼが酵素活性を有するようになります。引き続き、Smad anchor for receptor activation (SARA) とよばれるアダプタータンパク質がTGF-βシグナル伝達分子の特異型Smad (receptor-regulated Smad; R-Smad) であるSmad2及びSmad3をセリン・トレオニンキナーゼ酵素活性を持つTGF-βⅠ型受容体に提示することで、R-SmadのC末端セリン残基をリン酸化します。リン酸化されたR-Smadは、共有型Smad (Common partner Smad; Co-Smad) のSmad4と3者複合体を形成し、核に移行し、直接また他の転写因子を介して間接的に、TGF-βシグナルの直接標的遺伝子プロモーター内の特異的DNA配列に結合し、標的遺伝子の転写を制御しています(図3)。
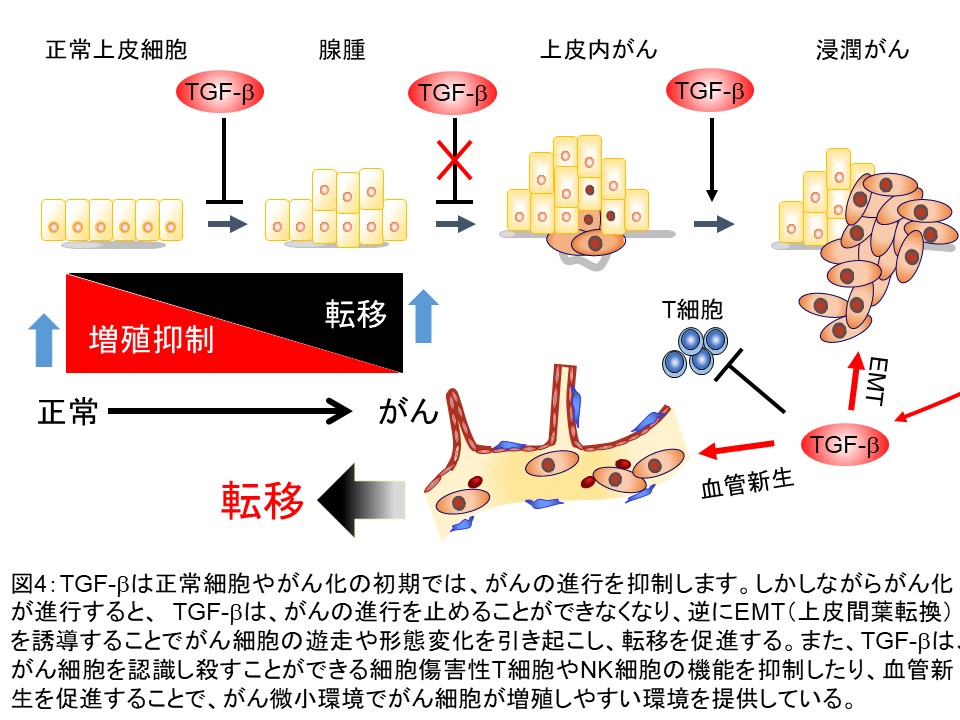
TGF-βは、がん化に関して二面性を有しているといわれています。正常上皮細胞やがん化初期の細胞は、TGF-βの持つ細胞増殖抑制作用により細胞増殖を抑制するので、がん細胞は増殖できません。一方、悪性化したがん細胞は、自らが多量に分泌したTGF-βがオートクライン(または他の近傍細胞からのパラクライン)によりEMT(上皮間葉転換)をおこすことで、運動能と共に転移能を獲得します。さらに、免疫監視システムを低下させることで、がん細胞が免疫監視システムから回避し、腫瘍内に新たな血管を作ること(腫瘍血管新生)を亢進し、がん細胞自身が増殖・転移しやすい微小環境を形成しています(図4)。
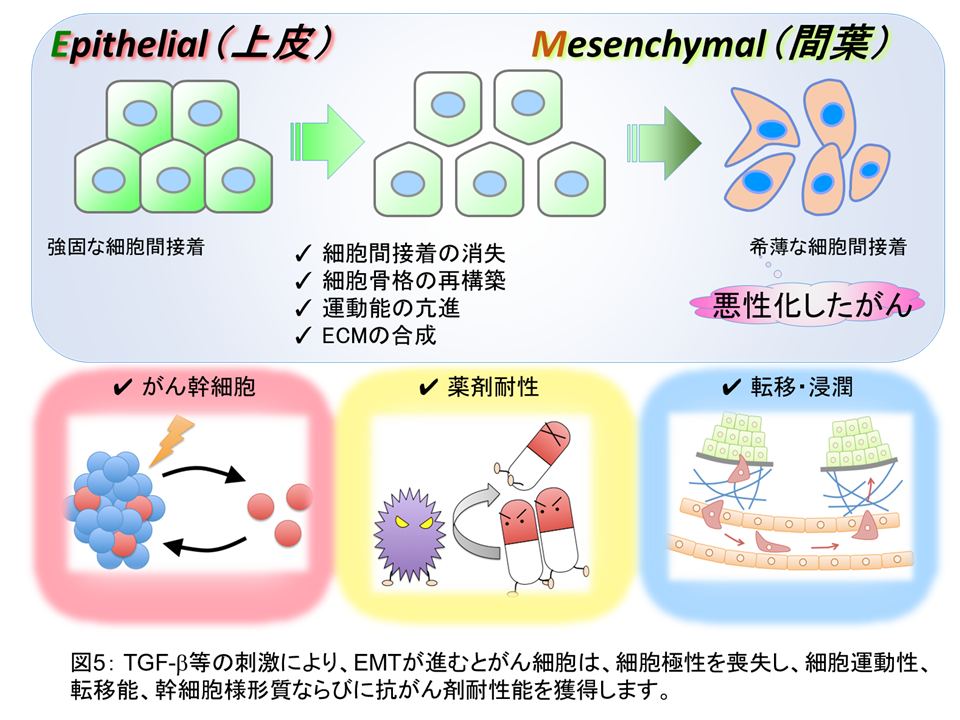
EMTとは、上皮細胞が間葉系細胞に変化する現象であり、正常な組織では発生過程の組織損傷や修復に重要なプロセスであります。一方、上皮組織系のがん細胞がEMTの進行に伴い、E-カドヘリンやクローディン1の発現を低下させ、N-カドヘリンやビメンチンの発現を亢進させます。この過程が進むとがん細胞は、細胞極性を喪失し、細胞運動能、転移能、幹細胞様形質ならびに抗がん剤耐性能を獲得します(図5)。そこで私たちは、EMT過程の分子機構の解明を目指すとともに、EMTを阻害するような‘くすり’の‘種(シーズ)’の開発を行っています。
昨今TGF-βが有するがん化促進作用を阻害することを目的とした抗がん剤創薬が進んでいます。例えば、抗TGF-β抗体やTGF-βを細胞外でトラップするようなTGF-βⅡ型受容体の細胞外領域のみを発現させたリコンビナントタンパク質などです。またニボルマブ(抗PD-1抗体)と抗TGF-β抗体の併用投与で、腫瘍組織に細胞傷害性T細胞が集積しやすくなり、がん細胞増殖を阻害するような知見も発表され、近年、抗PDL-1抗体と上述したTGF-βⅡ型受容体の細胞外領域を融合したリコンビナントタンパク質を用いた臨床研究も始まっています。
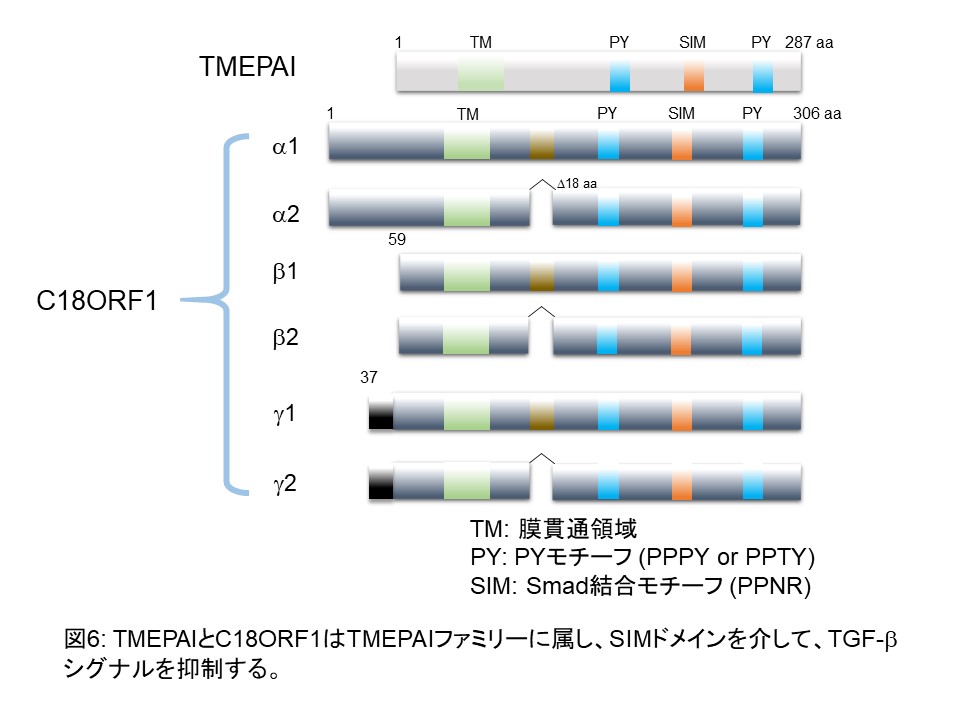
私たちは、TGF-βの直接の標的遺伝子の中で様々な腫瘍組織で発現が亢進していることが報告されているTMEPAI (TransMEmbrane Prostate Androgen-Induced RNA) 及びそのファミリー分子であるC18ORF1がTGF-βシグナルを特異的に抑制する分子について研究を行っています(図6)。TMEPAIとC18ORF1は、R-Smadとの結合に関してSARAと競合阻害することにより、SARAが充分量のR-SmadをTGF-βⅠ型受容体に提示できないようにします。そのためTGF-βⅠ型受容体セリンスレオニンキナーゼがR-Smadをリン酸化できなくなるために、TGF-βシグナルが抑制されるということを発見しました。
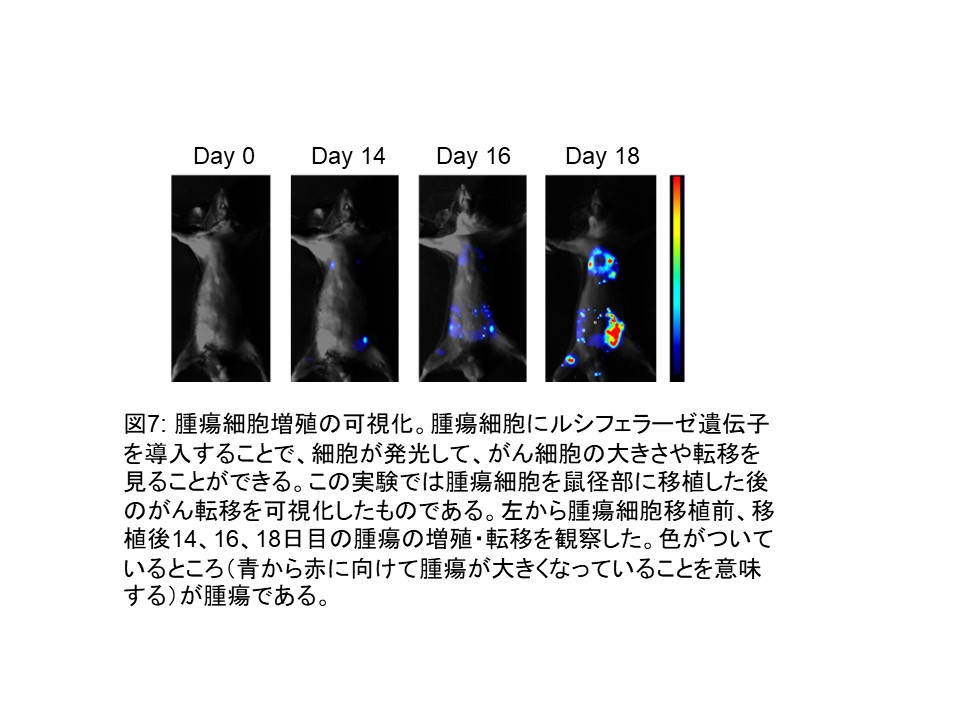
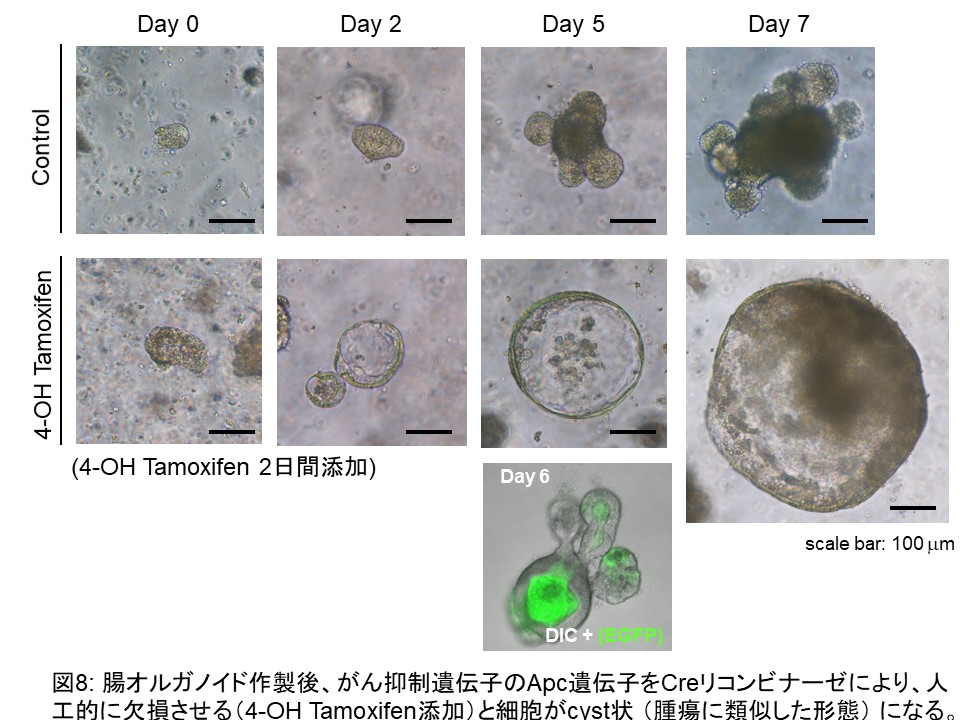
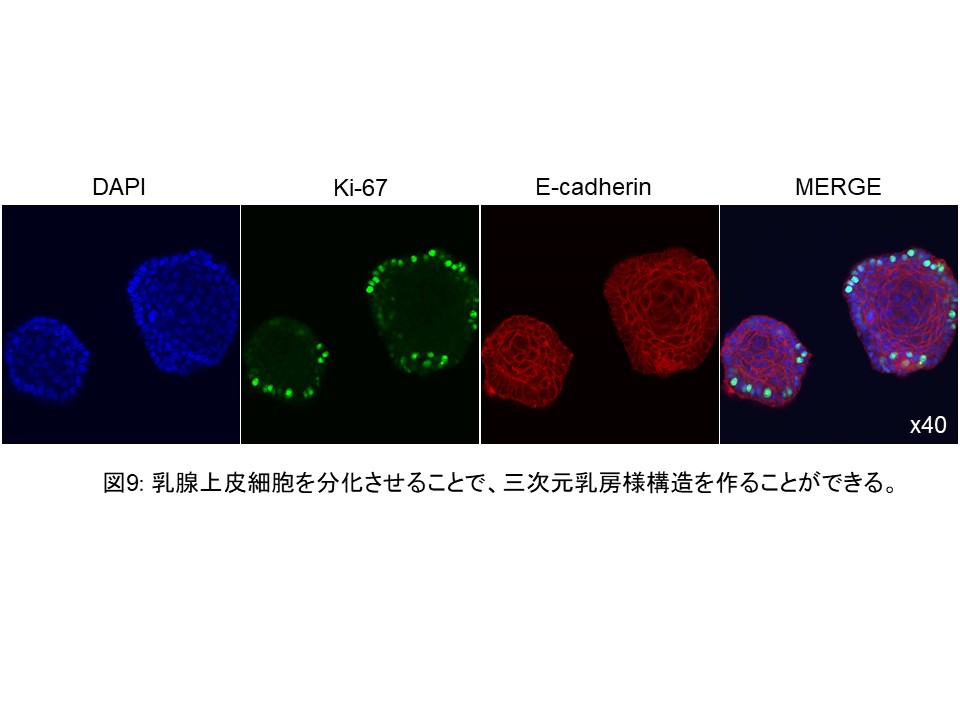
現在私たちは、このTMEPAIファミリーの機能をさらに詳細に検討し、TMEPAIががんの悪性化にどのように関与しているかを明らかにすべく、腫瘍形成を可視化、腸や乳腺のオルガノイド培養技術等を用いて、研究をしています(図7-9)。
その他の研究として私たちは、抗がん剤のシーズを探索しています。例えば、がん細胞で高発現または異常な機能を持つようになったタンパク質に対する低分子化合物を見つけ、プロテインノックダウン法とよばれる新たな手法を用いた創薬を目指す研究です。
現在私たちの研究室で行っている研究内容は以下の通りです。
①TGF-βファミリーによるがん進展制御機構の解明
②EMTの分子メカニズムの解明と抗がん剤開発
③プロテインノックダウン法に利用できる低分子化合物の同定と創薬への応用
大学院進学に興味のある学生さんは、いつでも遊びに来てください。